
聚焦健康中国 医药(第一健康报道北京 品宣)
近日,艾名医学、西湖大学附属杭州市第一人民医院、杭州市肿瘤医院、成都中医药大学等团队经过3年联合攻关,首次成功利用肺癌晚期患者的恶性积液,建立患者来源类器官(下文简称PDO)模型,无需患者本人“试药”便可准确预测靶向药的用药效果,总体准确率达87.1%,为晚期肺癌精准治疗搭建了全新的技术平台。该成果也已发表在国际肿瘤学领域的顶尖期刊《Cancer Letters》(2026, 645:218356)上。
此外,研究还首次发现:布洛芬可以逆转三代 EGFR#x2011;TKI 靶向药的耐药,为临床上解决耐药难题,提供了低成本、高可行性的新方向。

研发初衷:为“与死神的赛跑”争取“抢跑”的机会
肺癌目前是全球发病率和死亡率均排名第一的癌症,死亡病例约占全部癌症死亡病例的20%。在肺癌治疗中,较为常用的EGFR#x2011;TKI类靶向药容易出现耐药,一直是临床上最难解决的问题。对于患者来说,靶向药一旦发生耐药,便意味着开始 “和死神赛跑”——重做一系列检测,探寻耐药原因,重做治疗方案,开始新一轮治疗——而类器官技术,可以利用患者自体组织样本,在患者体外培育出癌变器官的若干份“副本”,替患者“试药”,不仅能提前预测治疗效果,更能在靶向药发生耐药后,及时给出新的治疗方案,这无异于给患者带来“抢跑”的机会。
然而临床一线却往往面临因患者身体状况等原因无法完成手术或穿刺活检,因而无法提取样本培育类器官模型,后续检测、治疗便无从下手。
为解决这一困境,2023 年,西湖大学附属杭州市第一人民医院、杭州市肿瘤医院、成都中医药大学和艾名医学的研发团队经多次研究讨论后开启课题,尝试不使用手术或穿刺从患者器官提取样本,转而从肺部恶性积液中建立可用于疗效预测和耐药研究的类器官模型平台。
然而,传统类器官制备如同“从零建高楼”,需先获取高质量肿瘤组织再进行培养,“原料”稀缺是首当其冲的问题。而使用细胞含量极少的肺部恶性积液,更使“原料困境”雪上加霜,是全球类器官领域公认的难点。
历经三年艰苦攻关,在团队通力协作下,科学家们解决了多个课题卡点:比如胸水样本红细胞污染严重,常规裂解法难以彻底清除,且易损伤肿瘤细胞活性;又如恶性积液中肿瘤细胞多以单细胞形式分散存在,直接培养难以自发聚集形成类器官等等。
艾名医学依托在肿瘤类器官体系构建方面的技术优势,与临床团队反复调试培养体系。最终创新采用Ficoll密度梯度离心联合低贴壁培养技术,既高效富集肿瘤细胞、保留细胞活性,又通过悬浮震荡促进单细胞自聚集成簇,最终将类器官培养成功率提升至82.8%,并建立了涵盖肺腺癌、鳞癌、小细胞肺癌等主要病理类型的生物样本库,最终实现从样本库建设,到精准用药指导再到耐药破解策略的全链条突破。
一位团队成员说,如果把晚期癌症患者比作溺水的人,那么团队的每一次实验,每一份数据,都会化成砖块垫在他脚下,让他离水面更近,离希望更近。他坚信,类器官技术已展现出巨大应用潜力,在不远的将来,癌症必将被人类攻克。


国内首台自研AI辅助全自动类器官系统培养鉴定智能工作岛OSCAR-AI,可实现同时测试100+种抗肿瘤药物效果,全流程无人值守自动化运行,跻身全球一流水平
临床意义:为晚期肺癌治疗带来新希望
据介绍,本研究中构建的恶性积液类器官模型及发现的耐药逆转策略,在临床检测、精准治疗、耐药研究、新药研发等维度具有重要的临床应用价值。
首先是为晚期肺癌提供微创、高效的体外检测方式。本研究证实恶性积液可作为PDO构建的理想样本来源,通过常规引流操作即可预判靶向药有效性。相比手术或穿刺活检,不仅具有微创、可重复取样的优势,且方案成功率高、构建周期短,能快速为晚期患者建立个性化体外模型,为患者减轻痛苦,节约时间。
其次是提升肺癌精准治疗的临床决策效率。传统基因检测仅能依据驱动基因突变选择药物,无法预测患者对药物的实际响应,而本研究下的 PDO 模型可直接在体外进行药物敏感性检测,总预测准确率达 87.1%,能为临床医生提供更精准的个性化用药指导。同时,PDO 可富集肿瘤细胞,发现原代样本中未检测到的耐药突变,弥补了传统基因检测的不足,为治疗方案调整提供依据。
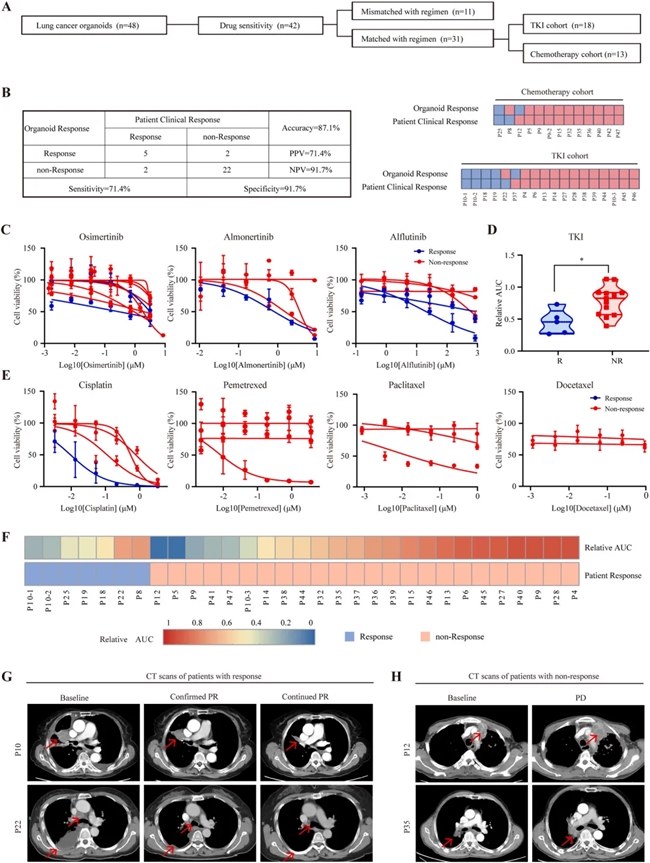
PDO 药物敏感性可精准预测临床治疗响应
此外,解析了三代 EGFR-TKI 耐药机制,提供潜在的临床联合治疗方案。本研究首次明确细胞外基质重塑、细胞周期失调、血管生成等通路是三代 EGFR-TKI 耐药的关键,为后续耐药靶点的开发提供了新的生物学视角。更重要的是,筛选出的布洛芬是临床常用的抗炎药,安全性高、价格低廉、可及性强,其与奥希替尼(一种三代EGFR-TKI靶向药)的协同作用为临床克服靶向药耐药提供了简单、可行的联合治疗方案,有望快速应用于临床。
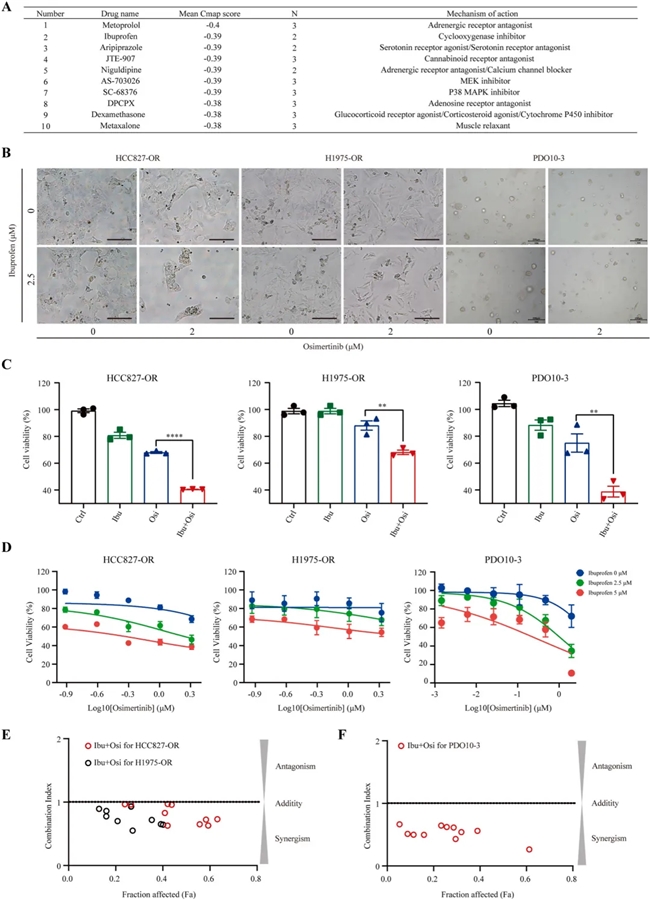
布洛芬与奥希替尼协同逆转 EGFR-TKI 耐药
最后,为肺癌药物研发和耐药研究提供全新平台。本研究下的PDO 模型能高度复刻患者肿瘤的病理和基因组特征,可作为个性化药物筛选和耐药机制研究的理想体外模型,不仅能用于已上市药物的敏感性检测,还能为新型抗肿瘤药物的研发提供高效的筛选平台,加速肺癌新药的研发进程。
补充阅读:什么是类器官
顾名思义,类器官即类似真实器官,是利用干细胞的自我更新和分化能力,在体外培养形成的一种微小组织器官类似物,在很大程度上具有体内相应器官的特征。类器官弥补了传统研究中细胞简单模型与动物复杂模型的不足,为生命体关键功能研究提供了重要实验基础,并在疾病机理研究、药物筛选、再生医学、生物材料评价等方面具有重大理论意义和应用前景,已成全球范围内的研究热点。科技部下发的《关于对“十四五”国家重点研发计划6个重点专项2021年度项目申报指南征求意见的通知》中,把“基于类器官的恶性肿瘤疾病模型”列为“十四五”国家重点研发计划中首批启动重点专项任务。
(责编 袁正杰)